Tout savoir sur les matériaux photochromiques
C’est quoi un matériau photochrome ?
Un revêtement photochrome (du grec photôs lumière et chromos couleur) est, par définition, constitué d’un pigment/colorant dont les propriétés optiques (couleurs) changent en présence d'une excitation lumineuse.
Ces composés photosensibles font partie de la vaste famille des matériaux X-chromes, à savoir des matières qui changent de couleurs sous l'influence d'un simulus extérieur : température, pression, taux d'humidité, etc.
Le mécanisme
 Plus spécifiquement, un pigment photosensible est une substance chimique, organique ou inorganique, dont la coloration est modifiée sous excitation lumineuse suite à la formation d'un état métastable. Ce phénomène peut être réversible ou non, et la cinétique est fortement dépendante du pigment et de la nature de l'excitation.
Plus spécifiquement, un pigment photosensible est une substance chimique, organique ou inorganique, dont la coloration est modifiée sous excitation lumineuse suite à la formation d'un état métastable. Ce phénomène peut être réversible ou non, et la cinétique est fortement dépendante du pigment et de la nature de l'excitation.
Le photochromisme est une transformation réversible, photo-induite dans au moins un sens, entre deux états A et B d’une espèce chimique ayant des spectres d’absorption différents. Le rayonnement électromagnétique responsable de la transformation selon le mécanisme se situe dans le domaine de l’ultraviolet, du visible ou du proche infrarouge.
Le passage A → B s’effectue par irradiation à une longueur d’onde λA correspondant au domaine spectral du photochrome (au niveau fondamentale A), et celui de B → A par irradiation à une longueur d’onde λB dans la zone d’absorption du photochrome (niveau photoinduit métastable B), ou par réaction thermique (Δ).
Si l’on considère la réaction de retour de B vers A, il existe deux types de photosensibles : - forme P, si le retour a lieu uniquement par photochimie ; - forme T, si le retour peut aussi avoir lieu par voie thermique.
Quelles sont les grandes familles de matériaux photochromes ?
Historiquement, la première description d’une propriété photosensible remonte à 1867. Fritzsche (C. R. l'Academie Sci. 1867, 69, 1035) rapporta la décoloration d’une solution de tétracène à la lumière du soleil, puis son retour à sa colorimétrie initiale (orange) dans le noir.
Aujourd’hui, le photochromisme est une propriété observée dans des molécules purement organiques, dans des dérivés biologiques (notamment associés au mécanisme de la vision rétinienne) mais aussi dans des composés inorganiques. Les réactions ne nécessitant pas de grandes modifications de conformation au cours de la photocommutation peuvent être observées aussi bien en solution qu'en phase cristalline.
Les matériaux organiques photochromiques
Ce sont certainement les molécules photochromes les plus étudiées. Les processus chimiques mis en jeu au cours de l’irradiation sont nombreux. Il peut s’agir d’un réorganisation structurale (isomérisation cis-trans autour de doubles liaisons, transfert de proton, ouverture et fermeture de cycles), comme d’un processus rédox.
Le photochromisme par réaction rédox a été découvert dans la famille des quinones et des naphtalènes (Z. F Phys. Chem., 1899, 30, 140). Dans ces systèmes, la transition photochromique est provoquée par la réaction rédox qui change fortement la conjugaison des arènes.
L’isomérisation cis-trans est rencontrée dans les dérivés des stilbènes, des azobenzènes. Ils présentent une isomérisation de la double liaison C=C ou N=N sous irradiation UV. Un exemple de photoisomérisation cis-trans est le « Disperse Red one » (DR1).
L’isomérisation par transfert de proton intramoléculaire est décrite pour les composés salicylidène-anilines. Le transfert de proton intramoléculaire permet le passage de la forme énol (jaune) à la forme cétone (rouge), en raison d’une transition n-p* de la paire d’électrons libres de l’oxygène. Selon les composés, le retour à la forme énol peut prendre quelques secondes ou plusieurs mois.
L’isomérisation par fermeture ou ouverture de cycle est un mécanisme rencontré sous deux formes :
- de forme T (réversibilité par voie thermique) comme les spiropyranes et spirooxazines
- de forme P (réversibilité par voie photochimique) comme les fulgides et les diaryléthènes
Les spiropyrannes et les spirooxazines ont été largement étudiées. Sous irradiation dans ultraviolet, la liaison carbone-oxygène se rompt, suivi d’une isomérisation cis-trans menant à la forme colorée appelée mérocyanine.
Les premiers exemples de diaryléthènes réversibles ont été décrits par Irie (J. Org. Chem. 1988, 53, 803-808). Cette famille est aujourd’hui largement étudiée. Les dérivés diaryléthènes allient à la fois une irréversibilité thermique et une grande résistance. Les cycles de photocoloration et de photodécoloration peuvent être effectués sur certains diaryléthènes plus de 104 fois sans observation de photodégradation (J. Org. Chem. 1988, 53, 6136-6138).
Matériaux photosensibles hybrides
Les ligands organiques à base d’antenne photochrome
De nombreux complexes hybrides sont composés d’une (ou plusieurs) antenne(s) photochrome(s) organique(s) reliée(s) à un ion métallique. C'est la réorganisation structurale de ces antennes par isomérisation et/ou cyclisation photo-induite est à l'origine de la modification de couleur.
Parmi les antennes photosensibles les plus décrites, on trouve les dérivés azobenzènes, spiropyranes, diaryléthènes ou quinones. Les ligands utilisés pour connecter le complexe métallique sont fréquemment la bipyridine, la terpyridine ainsi que la cyclopentadiényle substituée par un groupement azobenzène.
Si l’on considère à titre d’illustration les diaryléthènes associés à des complexes métalliques, les composés obtenus présentent la propriété photochromique grâce au mécanisme de photocyclisation du ligand. Les complexes décrits impliquent notamment le rhénium, platine et zinc.
Les pigments photochromes à changement de géométrie
L’exemple le plus marquant est le complexe de cuivre, [Cu(dieten)2](BF4)2 possédant deux ligands N,N-diéthyléthylènediamine (dieten). Sous irradiation, le complexe passe d’une conformation plan carré à une conformation légèrement distordue qui place le métal dans une conformation légèrement tétraédrique. La photocommutation du rouge au violet est stable plusieurs heures à une température de 35 K.
Les complexes photochromes à transition de spin
Certains complexes ont la particularité de changer d’état de spin en fonction d’une irradiation. Cette réorganisation électronique d'une configuration haut spin à bas spin peut être accompagnée d’une modification de la couleur. Il existe plusieurs types de transitions provoquées par l’irradiation. L'effet LIESST (Light-Induced Excited Spin State Trapping) est le processus photoinduit le plus étudié. Il a été observé pour la première fois en 1984 (Inorg. Chem. 1985, 24, 2174) dans le complexe de Fer(II) possédant six ligands propyltétrazole (ptz), [Fe(ptz)6](BF4)2.
 Les complexes photosensibles à valence mixte
Les complexes photosensibles à valence mixte
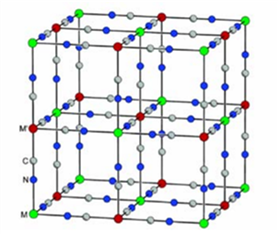
Certains analogues de Bleu de Prusse sont connus pour leurs propriétés photochrome et magnétique. Ces dérivés, composés de deux centres métalliques divalent et trivalent connectés par des ligands cyano, présentent une aimantation induite par irradiation ou pour des variations de températures. C’est notamment le cas des analogues cobalt-fer (Polyhedron 2001, 20, 1339) qui changent de la forme FeIIILS-CN-CoIIILS à la forme FeIILS-CN-CoIIHS par irradiation à basse température. Ce transfert d’électrons d’un centre métallique à l’autre s’accompagne d’une réorganisation structurale, d’une modification des propriétés optique (transition du vert au rouge) et magnétique.
Les complexes photoréactifs à intraconversion d’un ligand
Les composés de cette famille les plus étudiés sont les complexes présentant un ligand nitrosyle, à l’exemple du nitroprussiate de sodium : Na2[Fe(CN)5(NO)].
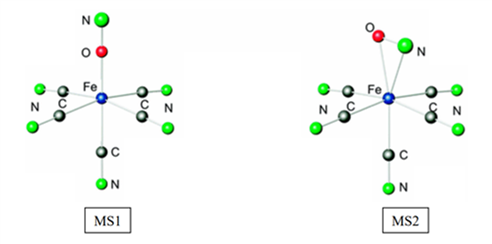 Ce complexe photosensible présente deux états métastables :
Ce complexe photosensible présente deux états métastables :
- un photoinduit MS1 qui se caractérise par l’inversion du nitrosyle en ligand isonitrosyle, où le métal est directement coordonné à l’oxygène.
- un photoinduit MS2, pour lequel le ligand nitrosyle linéaire au niveau fondamental devient « coudé ». Dans cette conformation dite coudée, la liaison métal-ligand est considérée comme une conformation η2 –NO.
Les pigments inorganiques photochromiques
L'effet photoinduit a également été décrit dans les pigments inorganiques, notamment, à base d’halogénures d’argent, de zinc et d’oxydes de molybdène.
Sous l’effet d’un rayonnement lumineux, la réaction oxydoréductrice, Ag+ + X-→ Ag0 + X0 (X = Cl, Br, I) entraîne la formation de colloïdes d'argent. Le matériau initialement clair devient gris sombre. Lorsque l'excitation cesse, la réaction inverse prend forme. Le matériau retourne dans sa configuration stable et recouvre sa coloration initiale.
Une autre classe de matériaux inorganiques photoréactifs est celle des oxydes à base de molybdène. Sous excitation UV, le MoO3 passe du jaune pâle à un bleu intense. Le changement de coloration est dû à la photo-réduction de cations métalliques Mo6+ (configuration 4d0) en Mo5+ (configuration 4d1) sous illumination.
Conclusion
A travers cette succincte analyse de l’existant, nous venons de rapporter les principaux matériaux et mécanismes responsables du photochromisme. Chacune de ces familles présentent des avantages et des inconvénients.
La propriété d’un système photochromique est dépendante du processus chimique engagé, et cinq facteurs principaux doivent être pris en compte :
- la nature de la source d'excitation : longueur d'onde, soleil ou lumière artificielle continue ou impulsionnelle, énergie,
- le taux de photoconversion,
- la durée de vie des états photoinduits,
- le domaine de température,
- la fatigabilité du processus.
Ces principaux facteurs varient selon la nature du processus chimique et de fait, selon la nature des molécules utilisées (organique, inorganique, biologique). Nos experts chimistes et photochimistes sont à votre disposition pour sélectionner le meilleur candidat au regard de la spécificité de votre cahier des charges et les applications.
![]()
NOUS CONTACTER
Nous revenons vers vous dans les meilleurs délais.
« * » indique les champs nécessaires

